Bazơ là gì? Bazơ được phân loại thành những dạng, cách đọc tên từng nhóm bazơ như thế nào? Tính chất của bazơ ra sao? Trong cuộc sống, bazơ có những ứng dụng nào và chúng ta thường gặp những loại bazơ nào quan trọng nhất?, …
Đối với hóa học, cùng với Axit thì bazơ như một phần của sự sống. Nó là điểm mấu chốt dùng để chứng minh và giải thích nhiều vấn đề phát sinh trong hóa học. Vì vậy, tìm hiểu kỹ về Bazơ là một điều vô cùng quan.
Hôm trước Công Ty Trung Sơn đã giới thiệu cho bạn những vấn đề xoay quanh Axit là gì? Và hôm nay chúng tôi sẽ đưa bạn đến một bài viết mới về bazơ là gì?
ĐỊNH NGHĨA BAZƠ LÀ GÌ? CÔNG THỨC CỦA BAZƠ
Định nghĩa về BAZƠ là gì?
Bazơ là hợp chất hóa học mà phân tử của nó bao gồm có một nguyên tử kim loại liên kết với một hay nhiều nhóm hidroxit (OH), trong đó hóa trị của kim loại bằng số nhóm hidroxit.
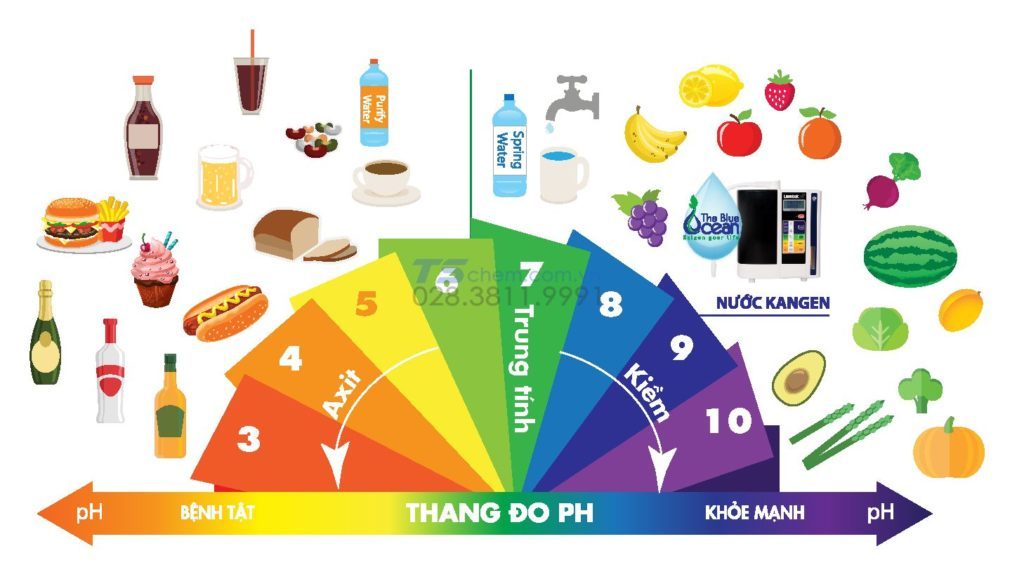
Ngoài ra, ta có thể hình dung bazơ chính là chất mà khi hòa tan trong nước sẽ tạo thành dung dịch có pH lớn hơn 7.
Công thức của BAZƠ là gì?
Bazơ có công thức hóa học tổng quát sau đây:
M(OH) n
Trong đó:
- M là môt kim loại
- n là Hóa trị của kim loại.
Ví dụ :
- CTHH của bazơ Natrihidroxit là NaOH
- CTHH của bazơ Sắt (III) hidroxit là H2CO3
- CTHH của bazơ kali hidroxit là KOH
PHÂN LOẠI BAZƠ VÀ CÁCH ĐỌC TÊN BAZƠ

Phân loại bazơ như thế nào?
Dựa vào tính chất hóa học, ta có thể chia thành:
- Bazơ mạnh như NaOH, KOH, …
- Bazơ yếu như Fe(OH)3, Al(OH)3…
Dựa vào tính tan của bazơ trong nước, người ta chia bazơ thành 2 loại:
- Bazơ tan được trong nước tạo thành dung dịch bazơ (gọi là kiềm):
- Ví dụ: NaOH, KOH, Ba(OH)2, Ca(OH)2, LiOH, RbOH, CsOH, Sr(OH)2.
- Những bazơ không tan:
- Ví dụ: Cu(OH)2, Mg(OH)2, Fe(OH)3, Al(OH)3…
- Bazơ tan được trong nước tạo thành dung dịch bazơ (gọi là kiềm):
Cách đọc tên bazơ như thế nào?
Bazơ được gọi tên theo trình tự:
Tên bazơ = Tên kim loại ( kèm hóa trị nếu kim loại có nhiều hóa trị ) + hidroxit
Ví dụ :
- NaOH được đọc là natri hidroxit
- Ca(OH)2 được đọc là canxi hidroxit
- Cu(OH)2 được đọc là đồng (II) hidroxit
- Fe(OH)2 được đọc là sắt (II) hidroxit.
TÍNH CHẤT VẬT LÝ CỦA BAZƠ
Những tính chất vật lý chung của các loại bazơ bao gồm:
- Bazơ nồng độ cao và bazơ mạnh có tính ăn mòn chất hữu cơ và tác dụng mạnh với các hợp chất axit.
- Bazơ sẽ gây ra cảm giác nhờn hoặc một số nhớt và có mùi
- Có vị đắng.
TÍNH CHẤT HÓA HỌC CỦA BAZƠ
Bazơ làm đổi màu giấy quỳ tím
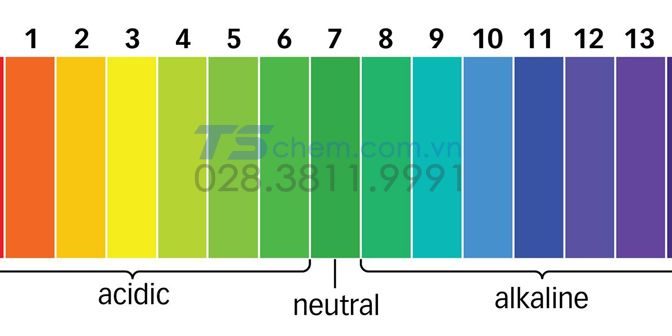
Ta thực hiện thí nghiệm nhỏ vài giọt dung dịch NaỌH vào giấy quỳ tím và sau đó quan sát ta nhận thấy rằng màu của nó thay đổi chuyển sang màu xanh. Do đó ta có thể kết luận rằng dung dịch Bazơ làm đổi màu giấy quỳ tím thành xanh.
Vì vậy, dựa vào tính chất này, giấy quì tím được dùng để nhận biết dung dịch bazơ.
Ngoài ra, Dung dịch bazơ còn làm phenolphthalein không màu đổi sang màu đỏ.
Dung dịch bazơ tác dụng với oxit axit tạo thành muối và nước
Phương trình phản ứng:
- 2NaOH + SO2 → Na2SO3 + H2O
- 3Ca(OH)2 + P2O5 → Ca3(PO4)2↓ + 3H2O
Bazơ (tan và không tan) tác dụng với axit tạo thành muối và nước.
Phương trình phản ứng:
- KOH + HCl → KCl + H2O
- Cu(OH)2 + 2HNO3 → Cu(NO3)2 + H2O
Bazơ tác dụng với nhiều dung dịch muối tạo thành muối mới và bazơ mới
Phương trình phản ứng:
- 2NaOH + CuSO4 → Na2SO4 + Cu(OH)2↓
Bazơ không tan bị nhiệt phân hủy thành oxit và nước
Phương trình phản ứng:
- Cu(OH)2 → CuO + H2O.
- 2Fe(OH)3 →Fe2O3 + 3H2O
ỨNG DỤNG CỦA BAZƠ TRONG ĐỜI SỐNG
- Trong ngành công nghiệp hóa chất, dược: Được sử dụng để sản xuất hay bán các sản phẩm có chứa gốc Sodium như Sodium phenolate (sản xuất thuốc Aspirin), Sodium hypochlorite (Javen) làm chất tẩy trắng, chất khử trùng, ….
- Được sử dụng làm hóa chất để xử lý đối với gỗ, tre, nứa,…để làm nguyên liệu sản xuất giấy dựa theo phương pháp Sulphate và Soda.
- Trong ngành công nghiệp dệt, nhuộm: Nhiều bazơ được sử dụng để làm chất phân hủy pectins, sáp trong khâu xử lý vải thô, khiến cho vải thêm bóng và nhanh hấp thụ màu cho vải nhuộm.
- Sử dụng bazơ để pha chế dung dịch tẩy rửa chai lọ, các thiết bị trong các nhà máy bia. Hoặc là dùng để pha chế dung dịch Kiềm nhằm xử lý rau, hoa quả trước khi chế biến hoặc đóng hộp chúng,…
Xem thêm: Kẽm Oxit Là Gì? Ứng Dụng Và Cảnh Báo Về Tính Độc Hại
MỘT SỐ BAZƠ QUAN TRỌNG PHỔ BIẾN THƯỜNG GẶP

Ta có thể gặp những bazơ phổ biến trong cuộc sống như:
- Amoniac (NH3) và các amin.
- Pyridin và các bazơ vòng thơm khác.
- Các hiđrôxít kim loại như hiđrôxít natri (NaOH) hay hiđrôxít kali (KOH).
- Nhiều ôxít kim loại tạo ra hiđrôxít bazơ với nước (anhiđrít).
Trong đó có 2 Bazơ quan trọng nhất bao gồm:
NATRI HIDROXIT (Xút ăn da)
Natri hidroxit là chất rắn không màu, tan vô hạn trong nước và có tính hút ẩm.
Natri Hidroxit có công thức hóa học NaOH và phân tử khối là 40
Dung dịch Natri hidroxit có tính nhờn làm bục vải, giấy và ăn mòn da.
Natri hidroxit có đầy đủ tính chất hóa học của 1 bazơ như:
- Làm quỳ tím đổi thành màu xanh.
- Làm phenolphthalein không màu đổi sang màu đỏ.
- Tác dụng với oxit axit tạo thành muối và nước 2NaOH + CO2 → Na2CO3 + H2O
- Tác dụng với axit tạo thành muối và nước. NaOH + HCl → NaCl + H2O
- Tác dụng với muối tạo thành muối mới và bazơ mới 2NaOH + FeSO4 → Na2SO4 + Fe(OH)2↓.
- Dung dịch NaOH có khả năng hoà tan : Al, Al2O3 , Al(OH)3
- NaOH có thể tác dụng với kim loại Be, Zn, Sb, Pb, Cr và oxit và hiđroxit tương ứng của chúng.
- Tác dụng với một số phi kim như Si, C, P, S, Halogen: Si + 2NaOH + H2O → Na2SiO3 + 2H2
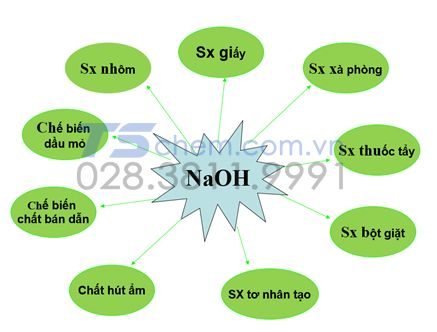
Ứng dụng của NaOH như sau : Sản xuất xà phòng, giấy, tơ nhân tạo, tinh dầu thực vật và các sản phẩm chưng cất dầu mỏ, chế phẩm nhuộm và dược phẩm nhuộm, làm khô khí và là thuốc thử rất thông dụng trong phòng thí nghiệm.
CANXI HIDROXIT
Canxi hidroxit hay còn gọi là vôi tôi.
Nó là một chất dạng tinh thể không màu hay bột màu trắng công thức hóa học là Ca(OH)2 và phân tử khối là 74.

Canxi hidro là một bazơ mạnh vì vậy nó có đầy đủ những tính chất của một bazơ như:
- Làm quỳ tím hóa xanh
- Làm phenolphthalein không màu đổi sang màu đỏ.
- Tác dụng với axit: tạo muối và nước.Ca(OH)2 + 2HCl → CaCl2 + 2H2O
- Tác dụng với oxit axit : Ca(OH)2 + CO2 → CaCO3 + H2O
- Tác dụng với dung dịch muối: Ca(OH)2 + Na2CO3 CaCO3 + H2O + CO2
Hyđroxit canxi có một số ứng dụng như:
- Chất kết bông trong xử lý nước, nước thải và cải tạo độ chua của đất.
- Thành phần của nước vôi, vữa trong xây dựng.
- Trong công nghiệp lọc dầu để sản xuất các phụ gia cho dầu thô (alkilsalicatic, sulphatic, fenatic)
- Trong công nghiệp thực phẩm để xử lý nước (để sản xuất các loại đồ uống như rượu và đồ uống không cồn),…
Tham khảo thêm bài viết: Tổng Quan Những Điều Bạn Cần Biết Về Natri Benzoat
NƠI MUA HÓA CHẤT UY TÍN
Hiện nay, nhu cầu sử dụng các loại axit, bazơ và nhiều hóa chất khác ngày càng tăng cao. Tuy nhiên, để đảm bảo an toàn khi sử dụng cũng như để đảm bảo cho kết quả như mong muốn, khách hàng nên lựa chọn cho mình những địa chỉ bán hàng tin cậy.
Tự hào là đơn vị có nhiều năm kinh nghiệm trọng lĩnh vực hóa chất và thiết bị thí nghiệm, Trung Sơn đã dần trở thành nơi gửi gắm niềm tin của nhiều khách hàng. Với giá cả phải chăng và hàng hóa đảm bảo chất lượng, chúng tôi sẽ mang đến cho bạn những sản phẩm tốt nhất. Hãy liên hệ ngay với chúng tôi khi có nhu cầu mua các sản phẩm hóa chất.
Bazơ bao gồm những chất hóa học mà ứng dụng của các chất đó đối với công nghiệp là vô cùng to lớn không thể phủ nhận được. Vì vậy hiểu biết khái sơ lược về BAZƠ là gì? BAZƠ được phân loại thành những dạng, cách đọc tên từng nhóm BAZƠ như thế nào? Tính chất vật lý và hóa học của BAZƠ ra sao? Trong cuộc sống, BAZƠ có những ứng dụng nào và chúng ta thường gặp những loại BAZƠ nào quan trọng nhất?,… là cực kỳ cần thiết.
Hi vọng bài viết trên đây của công ty Trung Sơn đã giúp bạn có thêm kiến thức về Bazơ là gì? Nếu bạn còn thắc mắc về bài viết ở bất kỳ điểm nào thì hãy ngay lập tức để lại bình luận ngay bên dưới để được chúng tôi hỗ trợ.



